Мутации генов, участвующих в репарации ДНК путем гомологичной рекомбинации (HRR)
- Для чего нужно знать статус мутаций в генах HRR?
- Какие биоматериалы нужно отправлять на HRR-тестирование?
- Какая доля пациентов с мКРРПЖ имеет мутации в генах HRR?
- Каким пациентам целесообразно выполнять HRR-тестирование?
- Каким методом выполняется HRR-тестирование?
Гены HRR – это группа генов, продукты которых участвуют в процессе репарации ДНК путем гомологичной рекомбинации (homologous recombination repair).
К этой группе относят, например, следующие гены:
| BRCA1 | BARD1 | CHEK1 | PALB2 | RAD51C |
| BRCA2 | BRIP1 | CHEK2 | PPP2R2A | RAD51D |
| ATM | CDK12 | FANCL | RAD51B | RAD54L |
Дефекты в этих генах могут приводить к нарушению репарации ДНК, увеличению геномной нестабильности и, тем самым, развитию рака (например, рака предстательной железы).
Как зарубежные, так и российские рекомендации указывают на целесообразность тестирования мутаций в некоторых генах HRR для пациентов с местнораспространенным или метастатическим РПЖ.
HRR-тестирование может выполняться в разном объеме, включая различные гены из числа участвующих в репарации ДНК путем гомологичной рекомбинации. Например, тест на мутации генов BRCA1/2 и ATM – частный случай HRR-тестирования.
Для чего нужно знать статус мутаций в генах HRR?
Наличие у пациента мутаций в некоторых генах HRR может сказать о многом:
| Прогноз | Тактика лечения | Обследование родственников | Внимание к другим видам рака |
|---|---|---|---|
| Результаты нескольких крупных ретроспективных исследований выявили связь между мутациями BRCA1/2 и агрессивным течением заболевания. Кроме того, наличие герминальной мутации BRCA2 оказывает негативное влияние на прогноз при мКРРПЖ. Также наблюдается плохой ответ на стандартную терапию при наличии в опухоли мутации в гене HRR. | Выявление мутаций может помочь определению тактики лечения | Если выявленная в гене BRCA/ATM мутация является наследственной, то целесообразно поискать ее у кровных родственников | Наследственная мутация BRCA/ATM приводит к развитию не только РПЖ, но и рака грудной и поджелудочной железы |
Какие биоматериалы нужно отправлять на HRR-тестирование?
На HRR-тестирование следует отправлять одновременно кровь и гистологический материал пациента.
Правила получения, хранения и транспортировки крови на HRR-тестирование – такие же, как для, например, BRCA-тестирования:
- Кровь необходимо собрать в пробирки с консервантом ЭДТА (с фиолетовой крышкой)
- До прибытия курьера кровь может храниться в холодильнике (при 2-8°С) до 3-х дней или в морозильнике (при ≤–18°С) – длительно
- Кровь можно транспортировать в лабораторию при комнатной температуре до 3-х дней
Для направляемого на HRR-тестирование гистологического материала кроме общих правил изготовления, подготовки и отправки блоков (эти правила можно посмотреть на стр. 6 в этой брошюре) следует учитывать дополнительные условия:
Какая доля пациентов с мКРРПЖ имеет мутации в генах HRR?
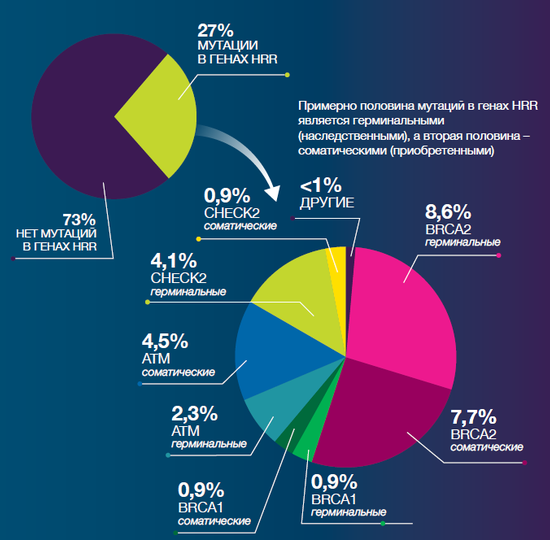
Частота мутаций в генах HRR при мКРРПЖ в России доподлинно неизвестна. По данным зарубежных исследований, мутация хотя бы в одном гене HRR найдётся примерно у 27% пациентов при тестировании блока и 14% – при тестировании крови. Иными словами, около половины мутаций генов HRR при мКРРПЖ – соматические, т.е. могут быть выявлены только при тестировании материала опухоли.
Большая часть мутаций генов HRR при мКРРПЖ приходятся на ген BRCA2. Значительная доля случаев HRRm-ассоциированного мКРРПЖ приходится на мутации генов ATM, CHEK2 и CDK12.
Каким пациентам целесообразно выполнять HRR-тестирование?
Согласно действующим клиническим рекомендациям Минздрава «Рак предстательной железы»:
Исследование на соматические мутации в потенциале позволит получить более полные результаты по сравнению с тестированием только герминальных мутаций. Тестирование опухоли на наличие соматических мутаций в генах BRCA1, BRCA2, ATM и других может быть рекомендовано для пациентов с местнораспространенным или метастатическим РПЖ.
В рамках Национальной Программы RUSSCO «Совершенствование молекулярно-генетической диагностики в Российской Федерации с целью повышения эффективности противоопухолевого лечения» HRR-тестирование выполняется для пациентов с метастатическим кастрационно-резистентным раком предстательной железы, которые получали или получают новые гормональные препараты (абиратерон/ апалутамид/ энзалутамид).
Каким методом выполняется HRR-тестирование?
В рамках Программы RUSSCO исследование HRR-мутаций выполняется методом NGS (секвенирования следующего поколения), который позволяет проанализировать все участки генов, мутации в которых могут приводить к потере их функции и, как результат, дефектам репарации путем гомологичной рекомбинации.
Если направленный в лабораторию гистологический материал пригоден для тестирования (содержит достаточное количество опухолевой ткани и позволяет получить пригодную для анализа ДНК), то HRR-тестирование выполняется по ДНК, выделенной из гистологического материала. Если поступивший в лабораторию гистологический блок для анализа непригоден, то тестирование проводится по крови.
В других лабораториях методы и материалы для исследования могут варьировать.
Нецелесообразно направлять образцы пациентов на широко распространенное исследование частых мутаций BRCA1/2 методом ПЦР, так как этот анализ выявляет в основном частые мутации в гене BRCA1, которые редки при раке предстательной железы.
![]() Благодарим ООО «АстраЗенека Фармасьютикалз» за спонсорскую поддержку проекта HRR-тестирования.
Благодарим ООО «АстраЗенека Фармасьютикалз» за спонсорскую поддержку проекта HRR-тестирования.
Список литературы:
- Министерство здравоохранения РФ. Клинические рекомендации. Рак предстательной железы. 2020.
- Castro E, et al. Eur Urol. 2015; 68: 186-193.
- Castro E, et al. J Clin Oncol. 2013; 31: 1748-1757.
- Mohler JL, et al. Prostate Cancer, Version 2.2019, NCCN Clinical Practice Guidelines in Oncology. J. Natl. Compr. Canc. Netw. 2019; 17, 479-505.
- Robinson D, Van Allen EM, Wu YM, et al. Integrative clinical genomics of advanced prostate cancer. Cell. 2015; 161(5): 1215-28.
- Grasso CS, Wu YM, Robinson DR, et al. The mutational landscape of lethal castration-resistant prostate cancer. Nature. 2012; 487(7406): 239-43.
- Annala M, et al. Cancer Discovery. 2018. doi:10.1158/2159-8290.CD-17-0937.
Войти
в базу данных
Для того, чтобы отправить материал на диагностику, вы должны быть зарегистрированным пользователем. Если у вас уже есть логин и пароль, то повторная регистрация не требуется.
в программе
Если вы новый пользователь, пожалуйста, пройдите процедуру регистрации.