Мутация гена BRAF при немелкоклеточном раке легкого
- Мутации гена BRAF у пациентов с немелкоклеточным раком легкого
- Эффективность BRAF/MEK ингибиторов для лечения взрослых пациентов с распространенным НМРЛ с мутацией гена BRAF V600
Мутации гена BRAF у пациентов с немелкоклеточным раком легкого
Согласно клиническим рекомендациям МЗ РФ, при выявлении неплоскоклеточного рака легкого рекомендуется проведение молекулярно-генетического исследования мутаций в гене EGFR (18-21-й экзоны), BRAF V600E, а также транслокаций генов ALK и ROS1 [1].
Примерно у 60% пациентов с НМРЛ выявляются мутации, в отношении которых может быть применена различная таргетная терапия [2-5]. В частности, у 2% пациентов с диагнозом рак легкого выявляется мутация BRAF V600 [6], причем зачастую она встречается при аденокарциноме. Гистологически НМРЛ с мутацией BRAF V600 характеризуется высокой агрессивностью опухоли [7].
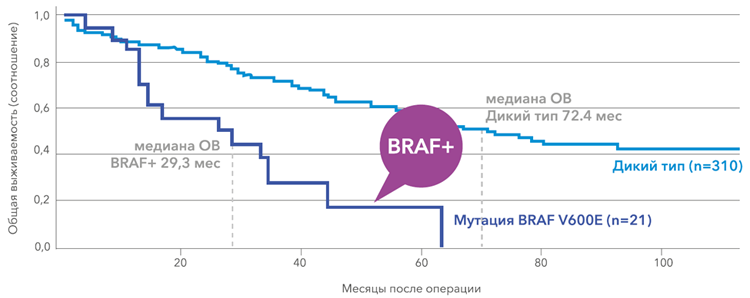
BRAF мутация – маркер неблагоприятного прогноза [8]
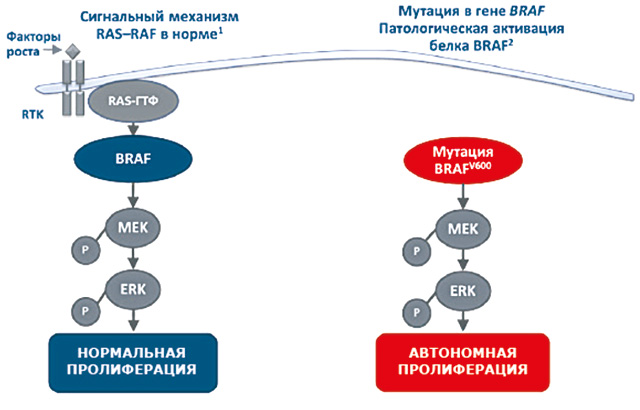
Сигнальный путь RAS/RAF/MEK/ERK играет важную роль в передаче внеклеточных сигналов в ядро клеток, что приводит к поддержке баланса роста/пролиферации и апоптоза клеток. Мутации, возникающие в генах белков сигнального пути RAS/RAF/MEK/ERK, приводят к развитию немелкоклеточного рака легкого (НМРЛ), меланомы и других видов злокачественных новообразований. Мутация BRAF вызывает конститутивную активацию данного сигнального пути, что приводит к неконтролируемому росту и пролиферации клеток [9].
Эффективность BRAF/MEK ингибиторов для лечения взрослых пациентов с распространенным НМРЛ с мутацией гена BRAF V600
Согласно клиническим рекомендациям МЗ РФ, при мутации BRAF V600E рекомендуется режим 1-й линии терапии – комбинация BRAF/MEK-ингибиторов: дабрафениба по 150 мг 2 раза в сутки внутрь ежедневно и траметиниба по 2 мг/сут. внутрь ежедневно до клинического прогрессирования или развития непереносимой токсичности [1].
Дабрафениб и траметиниб являются таргетными препаратами, подавляющими активность различных представителей семейства серин-треониновых киназ, а именно BRAF и MEK1/2 в сигнальном пути RAS/RAF/MEK/ERK [10].
Применение комбинации препаратов дабрафениб и траметиниб у пациентов с распространенным НМРЛ с мутацией в гене BRAF V600 основано на безопасности и эффективности дабрафениба в сочетании с траметинибом согласно результатам многоцентрового нерандомизированного открытого исследования II фазы, в котором участвовали пациенты с НМРЛ IV стадии с мутацией BRAF V600 (36 пациентов, ранее не получавшие химиотерапию, и 57 пациентов, ранее получавшие химиотерапию) [11].
Согласно 5-летним результатам наблюдения в рамках данного исследования были достигнуты высокие показатели выживаемости и частоты ответа независимо от того, получали пациенты терапию ранее или нет. Основные результаты исследования представлены в таблице [12].
| По оценкам исследователей | Первичные пациенты (n=36) |
Предлеченные пациенты (n=57) |
|---|---|---|
| ЧОО, % (95% ДИ) | 63,9 | 68,4 |
| Контроль заболевания, % (95% ДИ) | 75 | 80 |
| Медиана ВБП, мес. | 10,8 | 10,2 |
| Процент живых пациентов через 5 лет наблюдения, % | 22 | 19 |
| Медиана ОВ, мес. | 17,3 | 18,2 |
К наиболее распространенным нежелательным явлениям (частота возникновения более 20%) относились лихорадка, тошнота, рвота, периферический отек, диарея, сухость кожи, потеря аппетита, астения, озноб, кашель, усталость, сыпь и диспноэ [11].
Список литературы:
- Клинические рекомендации. Злокачественное новообразование бронхов и легкого. Год утверждения: 2021. Разработчик клинических рекомендаций: Ассоциация онкологов России, Общероссийская общественная организация «Российское общество клинической онкологии».
- Pamela Villalobos. Lung Cancer Biomarkers. Hematol Oncol Clin North Am. 2017 February; 31(1): 13–29.
- Pao W, Girard N. New driver mutations in non-small-cell lung cancer. Lancet Oncol. 2011; 12: 175-180.
- Paik PK, Arcila ME, Fara M, et al. Clinical Characteristics of Patients with Lung Adenocarcinomas Harboring BRAF Mutations. J Clin Oncol. 2011; 29: 2046-2051.
- Takeuchi, K, Soda M, Togashi Y, et al. RET, ROS1 and ALK fusions in lung cancer. Nature. 2012; 378-381.
- Kris MG, et al. JAMA. 2014; 311(19): 1998-2006.
- Lindeman, NI, et al. Molecular Testing Guideline for Selection of Lung Cancer Patients for EGFR and ALK Tyrosine Kinase Inhibitors. Arch Pathol Lab Med. 2013; 137: 828-1174.
- Marchetti, Journal of Clinical Oncology 29, no.26 (September 10, 2011) 3574-3579.
- Marchetti A, et al. J Clin Oncol. 2011; 29: 3574-3579.
- Cardarella S, et al. Clin Cancer Res. 19(16): 4532-4540.
- Planchard D, et al. Lancet Oncol. 2016; 17: 642-650;
Planchard D, et al. Lancet Oncol. 2016; 17: 984-993. - Planchard D, et al. Journal of Thoracic Oncology. 2022; 17: 103-115.
Войти
в базу данных
Для того, чтобы отправить материал на диагностику, вы должны быть зарегистрированным пользователем. Если у вас уже есть логин и пароль, то повторная регистрация не требуется.
в программе
Если вы новый пользователь, пожалуйста, пройдите процедуру регистрации.