Транслокации с участием гена ROS1
- Тестирование на наличие транслокации гена ROS1
- Зачем определять статус транслокации ROS1?
- Кому нужно проводить тестирование?
- Методы диагностики
Тестирование на наличие транслокации гена ROS1
Тест на наличие транслокации гена ROS1 показан больным распространенным немелкоклеточным раком легкого с отрицательным статусом мутаций EGFR и ALK для отбора пациентов на терапию кризотинибом. Тестирование ROS1 проводится пациентам ТОЛЬКО с ОТРИЦАТЕЛЬНЫМ РЕЗУЛЬТАТОМ ALK.
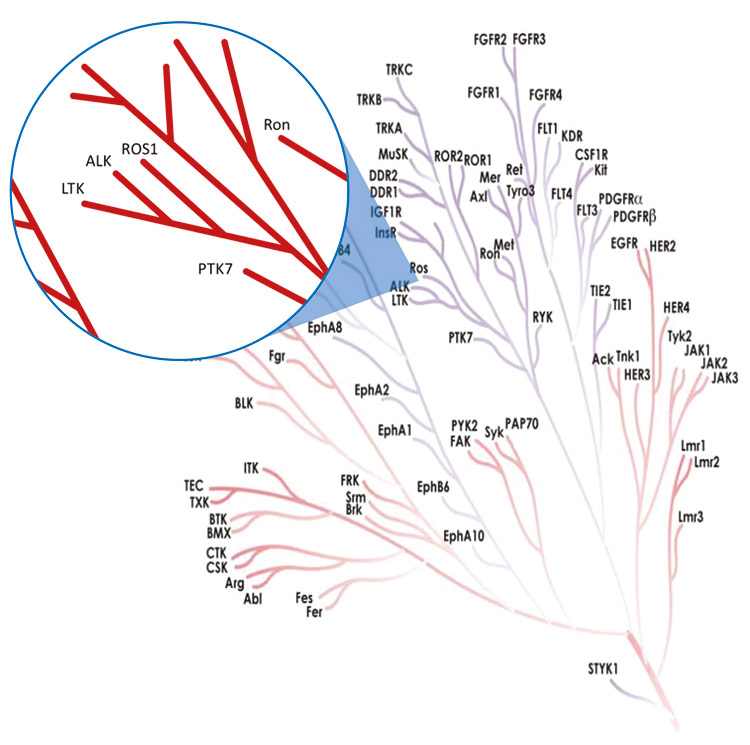
Онкоген ROS1 кодирует рецепторную тирозинкиназу, родственную киназе анапластической лимфомы (ALK) [16], а также ряду членов семейства инсулиновых рецепторов. ALK и ROS1 отвечают за синтез взаимосвязанных тирозинкиназ, АТФ-связывающие домены которых на 77% идентичны по аминокислотному составу (рис. 1).
Рисунок 1. Родственные киназы ALK и ROS1.
Реаранжировка приводит к слиянию части ROS1, которая включает полный домен тирозинкиназы, с 1 из 12 различных белков-партнеров.
Полученная в результате слияния тирозинкиназа ROS1 активируются конститутивно и обуславливает клеточную трансформацию.
Зачем определять статус транслокации ROS1?
Обнаружение транслокации ROS1 при немелкоклеточном раке легкого принципиально для проведения терапии таргетным препаратом кризотиниб, являющимся единственным зарегистрированным ингибитором тирозинкиназы ROS1.
Кому нужно проводить тестирование?
Реаранжировки ROS1 развиваются примерно у 1-2% пациентов с НМРЛ. Как и реаранжировки ALK, реаранжировки ROS1 чаще выявляются у пациентов, которые никогда не курили или у которых в анамнезе имеется курение в небольших количествах, и отмечаются гистологические признаки аденокарциномы.
Методы диагностики
Методика диагностики реаранжировки ROS1 полностью соответствует алгоритму выявления реаранжировки ALK и на сегодняшний день производится с использованием метода FISH, ИГХ и OТ-ПЦР. Важно помнить, что на генетическом уровне реаранжировки ALK и ROS1 редко развиваются в одной и той же опухоли, и каждая из них определяет уникальную подгруппу НМРЛ [21].
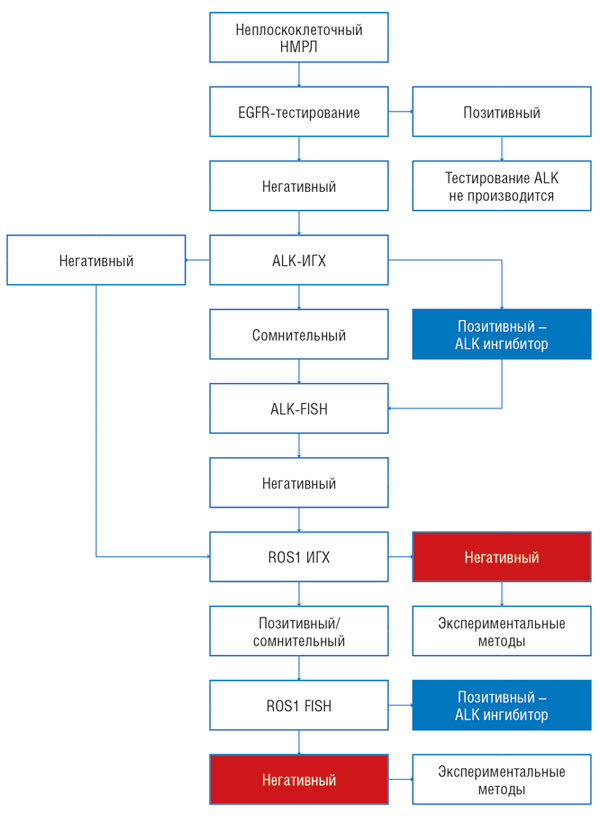
В рамках Программы алгоритм диагностики по выявлению транслокации ALK и ROS1 у пациентов с немелкоклеточным раком легкого представлен на рис. 2.
Рисунок 2. Алгоритм тестирования.
Список литературы:
- Soda M, Choi YL, Enomoto M, et al. Identification of the transforming EML4-ALK fusion gene in non-small-cell lung cancer. Nature. 2007; 448(7153): 561-566.
- Iwahara, T, Fujimoto J, Wen D, et al. Molecular characterization of ALK, a receptor tyrosine kinase expressed specifically in the nervous system. Oncogene 1997, 14: 439-449.
- Stoica, GE, Kuo A, Aigner A, et al. Identification of anaplastic lymphoma kinase as a receptor for the growth factor pleiotrophin. J. Biol. Chem. 2001; 276: 16772-16779.
- Bai RY, Ouyang T, Miething C, et al. Nucleophosmin-anaplastic lymphoma kinase associated with anaplastic large-cell lymphoma activates the phosphatidylinositol 3-kinase/Akt antiapoptotic signaling pathway. Blood 2000; 96: 4319-4327.
- Marzec M, Kasprzycka M, Liu X, et al. Oncogenic tyrosine kinase NPM/ALK induces activation of the rapamycin-sensitive mTOR signaling pathway. Oncogene 2007; 26: 5606-5614.
- Medves S, Demoulin JB. Tyrosine kinase gene fusions in cancer: translating mechanisms into targeted therapies. J. Cell. Mol. Med. 2012; 16(2): 237-248.
- Crystal AS, Show AT. Variants on a Theme: A Biomarker of Crizotinib Response in ALKPositive Non–Small Cell Lung Cancer. Clin Cancer Res 2012; 18(17): 4479-81.
- Horn L, Pao W. EML4-ALK: Honing In on a New Target in Non–Small-Cell Lung Cancer. J Clin Oncol 2009, 27(26): 4232-4235.
- Camidge DR, et al. Activity and safety of crizotinib in patients with ALK-positive nonsmall-cell lung cancer: updated results from a phase 1 study. Lancet Oncol 2012; 13: 1011-1019.
- Kim, et al. Updated Results of a Global Phase II Study with Crizotinib in Advanced ALK-positive Non-small Cell Lung Cancer. ESMO 2012; Abstract 1230PD.
- Food and Drug Administration. Summary review (application number: 202570Orig1s000). Food and Drug Administration 2011, Silver Spring.
- Camidge DR, Hirsch FR, Varella-Garcia M, Franklin WA. Finding ALK-positive lung cancer: what are we really looking for? J Thorac Oncol. 2011; 6(3); P.411-3.
- Meno-Kenudson M, Chirieac LR, Law K, et al. A novel, highly sensitive antibody allows for the routine detection of ALK-rearranged lung adenocarcinomas by standard immunohistochemistry. Clin Cancer Res. 2010; Vol.1; No.16(5; P.1561-71.
- Sanders HR, Li HR, Bruey JM, et al. Exon scanning by reverse transcriptase-polymerase chain reaction for detection of known and novel EML4-ALK fusion variants in non-small cell lung cancer. Cancer Genet. 2011; Vol.204; No.1; P.45-52.
- Lindeman NI, Cagle PT, Beasley MB, Chitale DA, Dacic S, Giaccone G, Jenkins RB, Kwiatkowski DJ, Saldivar JS, Squire J, Thunnissen E, Ladanyi M. Molecular Testing Guideline for Selection of Lung CancerPatients for EGFR and ALK Tyrosine Kinase Inhibitors. Guideline from the College of American Pathologists, International Association for the Study of Lung Cancer, and Association for Molecular Pathology. J Mol Diagn. 2013 Jul; 15(4): 415-53. doi: 10.1016/j.jmoldx.2013.03.001. Epub 2013 Apr 4. P.21-24.
- Acquaviva J, Wong R, Charest A. The multifaceted roles of the receptor tyrosine kinase ROS in development and cancer. Biochim Biophys Acta 2009; 1795: 37-52.
- Charest A, Lane K, McMahon K, et al. Fusion of FIG to the receptor tyrosine kinase ROS in a glioblastoma with an interstitial del(6)(q21q21). Genes Chromosomes Cancer 2003; 37: 58-71.
- Rikova K, Guo A, Zeng Q, et al. Global survey of phosphotyrosine signaling identifies oncogenic kinases in lung cancer. Cell 2007; 131: 1190-203.
- Gu TL, Deng X, Huang F, et al. Survey of t yrosine kinase signaling revea ls ROS kinase fusions in human cholangiocarcinoma. PLoS One 2011; 6(1): e15640.
- Davies KD, Doebele RC. Molecular pathways: ROS1 fusion proteins in cancer. Clin Cancer Res 2013; 19: 4040-5.
- Gainor JF, Shaw AT. Novel targets in non-small cell lung cancer: ROS1 and RET fusions. Oncologist 2013; 18: 865-75.
Войти
в базу данных
Для того, чтобы отправить материал на диагностику, вы должны быть зарегистрированным пользователем. Если у вас уже есть логин и пароль, то повторная регистрация не требуется.
в программе
Если вы новый пользователь, пожалуйста, пройдите процедуру регистрации.